ההבדל בין מים קשים מים כבדים | מים קשים לעומת מים כבדים
ההבדל העיקרי - מים קשים לעומת מים כבדים
ההבדל העיקרי בין מים קשים מים כבדים הוא הרכב שלהם כמו שני סוגים, "מים קשים" ו "מים כבדים" מתייחסים למים עם שני אטומי מימן ואטום חמצן אחד במולקולת המים. כאשר אנו רואים את ההרכב המולקולרי של מים כבדים , הוא מכיל יותר אטומי דוטריום מאשר אטומי מימן. ההרכב המולקולרי של מים קשים זהה למים הרגילים, אך ההרכב המינראלי (מגנזיום-מג והקלציום - Ca) הוא גבוה מ - מים רכים. -> -> מה זה מים כבדים? מולקולת מים מכילה שני אטומי מימן ואטום חמצן. מימן יש שלושה איזוטופים; פרוטיום (99. 98%), דאוטריום וטריטיום. פרוטיום יש אלקטרון אחד ונויטרון אחד. לדוטריום יש נויטרונים בגרעין בנוסף לאלקטרון ולפרוטון. דאוטריום הוא כפליים כפליים מאטום המימן השופע ביותר.
מים כבדים מכילים כמות גדולה של אטומי דויטריום מאשר אטום המימן הרגיל. לכן, המשקל המולקולרי שלה ואת הצפיפות גבוהה יותר מאשר המים הרגילים. הוא אמר כי צפיפות של מים כבדים הוא פי 11 יותר מזה של מים רגילים.מדגם היסטורי של "מים כבדים", ארוז בקפסולה חתומה.
מה זה מים קשים?
באופן כללי, מים מכילים כמות מסוימת של מינרלים כגון מגנזיום, סידן ואשלגן. אבל, מים קשים מכיל יותר מינרלים, במיוחד מגנזיום (Mg) וסידן (Ca) מאשר מים רגילים (מים רכים). בשל עובדה זו, הקשיות של המים הקשים גדולה יותר מאשר הקשיות של המים הרגילים. זה קורה כאשר המים פני השטח זורם דרך האדמה לתוך שכבת מי התהום על ידי המסת המינרלים במים זורמים חופשי.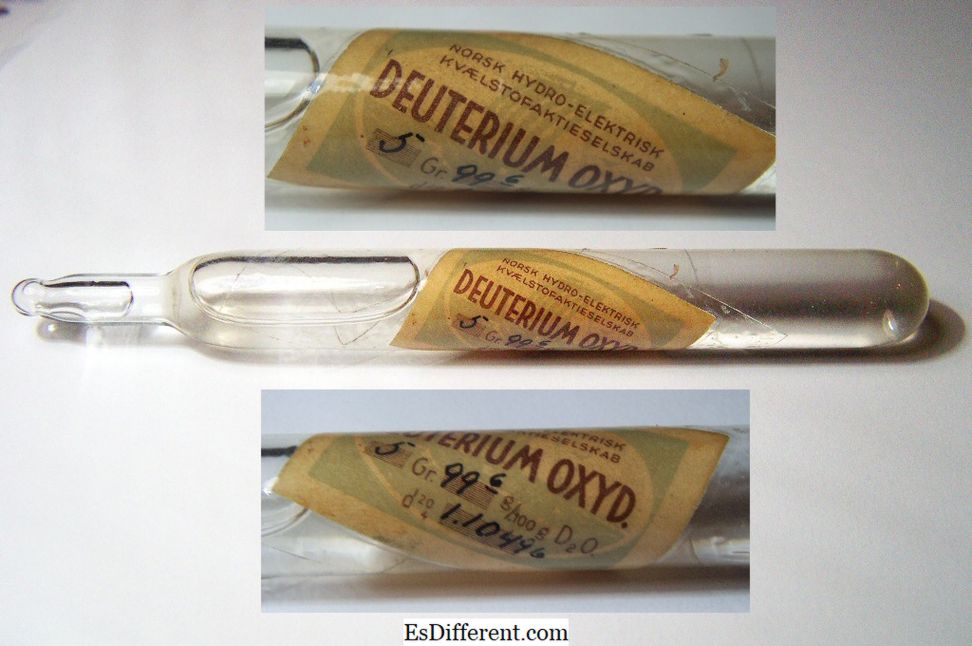
מים קשים אינם גורמים להשפעה מזיקה על בריאות האדם, אך הם גורמים לבעיות רבות נוספות כגון השארת פיקדונות צבעוניים לבנים בציוד בישול או רותחים, רצפות אמבטיה ובצינורות מים.
מה ההבדל בין מים קשים לבין מים כבדים?
הגדרת מים קשים ומים כבדים
מים כבדים:מים כבדים הם מים המכילים חלק ניכר של אטומי דוטריום, המשמשים כורים גרעיניים

מים קשים:
מים קשים הוא מים המכילים כמות ניכרת של מלחים מומסים של סידן ומגנזיום.
תכונות מים כבדים ומים כבדים קומפוזיציה
מים כבדים: מים כבדים מכילים חלק גדול של דאוטריום (מכיל נויטרונים נוספים בגרעין) אטומים מאשר המים הרגילים.הוא מכיל שני אטומי מימן ואטומי דויטריום המרכיבים את מולקולות המים שיש להן את הנוסחה המולקולרית כמו D
2
O (תחמוצת דאוטריום) ו- HDO (תחמוצת מימן-דוטיום).
מים קשים: ברמה המולקולרית, ההרכב של מים קשים דומה לזו של מים רגילים (H 2 O). אבל, הוא מכיל יותר מינרלים; מגנזיום וסידן מאשר מי השתייה הרגילים.
תכונות פיסיקליות וכימיות מים כבדים: תכונות פיסיקליות וכימיות של מים כבדים דומים למים הרגילים, אך יש לו ערך בצפיפות גבוהה. המשקל המולקולרי של המים הכבדים אינו מראה שינוי משמעותי משום שאטום החמצן היחיד תורם כ -89% למשקל המולקולרי. תכונות ביולוגיות של מים כבדים שונים מן המים הרגילים. מים קשים:
קשיחות היא הנכס העיקרי אשר שונה באופן משמעותי מן המים הרגילים.
סיווג USSS של קשיות מים - diff מאמר בינוני לפני טבלה ->
קשיות / mgl -1> טבע המים
0-60
מים רכים| 61- 120 קשה למדי מים | 121- 180 |
| מים קשים | <180 |
| מים קשים מאוד | הגבלה המומלצת של קשיות במי שתייה היא 80-100 מ"ג |
| -1 | אפקט בריאותי < מים כבדים: |
| כמות מסוימת של דאוטריום נמצא בגוף האדם, אך כמות גדולה של דאוטריום גורמת להשפעות בריאותיות מזיקות בגוף האדם, היא יכולה אפילו לגרום למוות. | מים קשים: |
מים קשים לא גורם השפעות בריאותיות בגוף האדם, אבל זה גורם לבעיות אחרות כגון חסימת צינורות מים והשארת משקעים מינרליים על תנורי חימום, ציוד בישול ורצפות האמבטיה. כדי להתגבר על בעיות אלה נגרמת על ידי מים קשים, מינרלים מוסרים. זה נקרא ריכוך. השיטה הנפוצה ביותר בשימוש יעיל הוא יון חילופי שרפים כמו מרכך. תמונה באדיבות:
"dripping barucet 1" על ידי משתמש: Dschwen - עבודה משלו. (CC BY-SA 2. 5) באמצעות ויקיפדיה
"תחמוצת דאוטריום Norsk" על ידי Alchemist-hp (שיחה) (www. Pes-mendelejew. (FAL) דרך



