ההבדל בין סיגמה לבין אג"ח פי ההבדל בין
מהו אג"ח סיגמא?
קשרים סיגמא הם קשרים בין אטומים בתוך מולקולות שנוצרו לאורך ציר המחבר את הגרעינים של האטומים של האטומים.
מולקולרית קשרים
מולקולות טופס כאשר אטומים להחליף או לחלוק אלקטרונים באמצעות מליטה כימית. יש בעצם שלושה סוגים של אג"ח. אג"ח יוניות, קשרים מתכתיים ואג"ח קוולנטיים. באג"ח יוניות, האטומים פשוט יחליפו אלקטרון כך שאטום אחד יהפוך לטעון חיובי והשני טעון בצורה שלילית, מה שיגרום להם להימשך על ידי הכוח האלקטרומגנטי. באגודות מתכתיים, האלקטרונים יחולקו באופן אחיד באמצעות המולקולה כולה ויוצרים ים של אלקטרונים חופשיים, דקלוקליים, המעטפים יונים טעונים באופן חיובי, הנמשכים אל האלקטרונים.
בתוך קוולנטיים, אלקטרונים משותפים והאופן שבו הם משותפים הוא דרך עננים הסתברות של האלקטרונים, ואת האורביטלים שבהם הם ממוקמים, חופפים באופן שהוא סימטרי בערך.
אורביטלים ואגודות סיגמא
אורביטלים הם אזורים סביב אטומים הקשורים לרמות אנרגיה מסוימות. אלקטרונים באורביטלים הרחוקים יותר מן הגרעין יהיו בעלי אנרגיה רבה יותר מאשר אלקטרונים באורביטלים הקרובים יותר לגרעין. כאשר האורביטלים של אטום אחד חופפים עם האורביטלים מאטום אחר, הם יוצרים אורביטלים מולקולריים המאפשרים קשרים מולקולריים המאפשרים, כמובן, מולקולות.
האג"ח סיגמא הם סוג הראשון של הקשר שייווצר בין אטומים. בתוך קשר סיגמא, ענני ההסתברות של האלקטרונים יהיו לאורך הציר המחבר בין גרעיני האטומים המחוברים. אג"ח סיגמא יהיה בדרך כלל טופס כאשר s אורביטלים מאטומים שונים חופפים ליצור קשר. הם תמיד ייווצרו לאורך הציר בין שני הגרעינים משום שהמסלול המסלול מסודר במשהו כמו כדור סביב הגרעין. -> -> סיגמא קשרים ואורביטלים סיגמא
האלקטרונים המרכיבים את הקשר סיגמה יהיה בתוך האורביטלים סיגמא וכך יהיה איפשהו לאורך ציר המחבר את הגרעינים של אטומים מלוכדות. הקשר sigma יכול, עם זאת, להיות יציב או יציב, תלוי אם האלקטרונים נמצאים סיגמה מליטה או מסלולית או מליטה נגד מליטה.סיגמה מליטה אורביטלים יהיה במרחב בין הגרעינים ואילו אנטי מליטה אורביטלים יהיה לאורך ציר המחבר את הגרעינים אבל על הצדדים של האטומים מול המרווח ביניהם. הקשר של הסיגמה יהיה יציב אם יותר אלקטרונים נמצאים במילואים מליטה ובלתי יציבים אם הם נמצאים יותר אורביטלים antibonding או אם יש מספר שווה של אלקטרונים בשניהם.
מהו הקשר של פיי?
pi bonds הם קשרים בין אטומים בתוך מולקולות שבהן האלקטרונים נמצאים מעל ומתחת לציר המחבר את גרעיני האטומים המצורפים, אך לא לאורך הציר.הם סוג השני של הקשר אשר ייווצר בתוך מולקולה לאחר הקשר sigma.
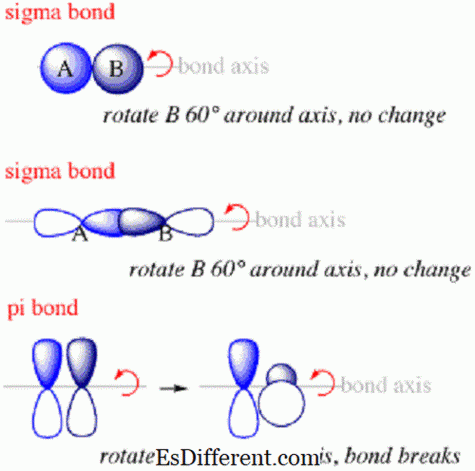
pi bond and
p
אורביטלים הסיבה לכך שקשורי pi נוצרים מעל ומתחת לציר ההידבקות, אך לא לאורך זה, משום שהם נוצרים בדרך כלל מחילופים חופפים כגון p
אורביטלים על האטומים מלוכדות. לאורביטלים אלה אין צפיפות אלקטרונים בגרעין. כתוצאה מכך, האלקטרונים המרכיבים את הקשרים הפיי הנוצרים מן האורביטלים החופפים של האורביטלים יהיו תמיד מקבצים באזור שאינו צמוד ישירות לגרעין. כמו כן, ניתן ליצור קשרים בין אורביטלים אטומיים אחרים, כדוגמת d אורביטלים בעלי תכונות משותפות עם p אורביטלים. py bonds and py orbitals כאשר p אורביטלים של אטומים שונים חופפים, הם יוצרים אורביטלים פי מולקולריים המאפשרים ליצור קשרים pi. הקשר יכול להיות שוב יציב או יציב, תלוי במסלול שבו נמצא האלקטרון. הקשר pi יהיה יציב אם יותר אלקטרונים נמצאים אורביטלים pi מליטה. זה יהיה יציב אם יותר נמצאים במיתרים נגד מליטה או אם מספר שווה הם שניהם.
קווי דמיון בין אג"ח סיגמה ואג"ח pi
איגרות חוב של סיגמא ואגפי pi מבוססות על אורביטלים מולקולריים ספציפיים הנגזרות מחפיפה בין מסלול אורביטלי אטומי מסוים, לדוגמה, אורביטלים של s של אג"ח סיגמא ו
p
אורביטלים במקרה של אג"ח pi. הם גם יכולים להיות יציבים או לא יציבים, תלוי אם אלקטרונים הם במולקולות מולקולרית מליטה או נגד מליטה אורביטלים מולקולריים. ההבדלים בין האג"ח סיגמא ואג"ח pi למרות הדמיון שלהם, ישנם הבדלים חשובים. אלקטרונים המרכיבים את האג"ח סיגמה יחולקו במרחב לאורך ציר המחבר את הגרעינים הצטרפו בעוד אלקטרונים בתוך אג"ח pi יחולקו מעל ומתחת לציר אבל לא לאורך זה. אג"ח סיגמא הן הקשרים הראשונים שנוצרים בין האטומים בתוך המולקולות ואילו האג"ח של פיי הם השני.
אג"ח סיגמא נוצרות לעיתים קרובות על ידי שילוב של
s
- אורביטלים באטומים שונים ואילו אג"ח pi נוצרות משילוב של
- p
- ואורביטלים דומים באטומים שונים. בנוסף, הכיוון של אורביטלים חופפים היוצרים אג"ח pi יהיה מאונך לזה של חופפים חופפים היוצרים אג"ח סיגמא. סיגמא אג"ח לעומת אג"ח pi סיגמה הקשר פי האג"ח
- אורביטלים אטומיים חופפים לאורך ציר מליטה



