ההבדל בין פניל לבנזיל | פניל לעומת Benzyl
פניל לעומת בנזיל
הן פניל והן בנזיל נגזרים מבנזין, ומבולבלים בדרך כלל על ידי תלמידי הכימיה. פניל הוא מולקולה פחמנית עם הנוסחה C 6 H 5 , ואילו בנזיל הוא C 6 H 5 CH 2 <; עוד CH 2 קבוצה מחוברת לטבעת הבנזן. Phenyl

6 H 5 . זה נגזר בנזין, ולכן, יש תכונות דומות כמו בנזן. עם זאת, זה שונה מבנזן בשל חוסר אטום מימן אחד פחמן. אז המשקל המולקולרי של פניל הוא 77 גרם mol -1 . Phenyl הוא מקוצר כמו Ph. בדרך כלל פניל מחובר לקבוצת פניל אחרת, אטום, או מולקולה (חלק זה ידוע כקבוצה החלופית, R כמו בדמות). אטומי הפחמן של פניל הם sp2 הכלאה כמו בבנזין. כל הפחמנים יכולים ליצור שלוש אגודות סיגמא. שניים מאגפי הסיגמא נוצרים עם שני פחמנים סמוכים, כך שיגרום ליצירת טבעת. הקשר סיגמא השני נוצר עם אטום מימן. עם זאת, בפחמן אחד, בזירה, הקשר של סיגמא השלישי נוצר עם אטום או מולקולה אחרת במקום אטום מימן. האלקטרונים של אורביטלים p חופפים זה עם זה כדי ליצור את ענן האלקטרון delocalized. לכן, פניל יש C- C באורכים דומים בין כל הפחמנים, ללא קשר שיש לסירוגין יחיד וקישור כפול. זה C-C אורך האג"ח הוא על 1. 4 Å. הטבעת היא מישורית ויש לה זווית של 120 ° בין הקשרים סביב פחמן. בשל הקבוצה החלופית של פניל, את הקוטביות ואת תכונות כימיות או פיסיקליות אחרות לשנות. אם החלופה תתרום אלקטרונים לענן האלקטרון הדלוקאלי של הטבעת, אלה ידועים כקבוצת אלקטרונים התורמת (E. g. -OCH 3 , NH 2 ). אם החלופית מושכת אלקטרונים מענן האלקטרון, היא ידועה כמסרת אלקטרונים. (E. G. -NO 2 , -COOH). קבוצות Phenyl יציבים בשל הארומטיות שלהם, כך שהם לא בקלות לעבור חמצון או הפחתות. יתר על כן, הם הידרופובי ולא קוטבי. -> ->
Benzylהנוסחה של בנזיל היא C
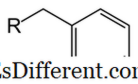
6 H 5 CH 2 . זהו גם נגזרת של בנזן. לעומת פניל, benzyl יש CH 2 קבוצה המצורפת טבעת בנזן. חלק אחר של המולקולה (R, כפי שמוצג בתמונה), יכול להיות קשור לקבוצת בנזיל באמצעות מליטה ל- 2 אטום פחמן. Benzyl הקבוצה מקוצר כמו "Bn". המשקל המולקולרי של קבוצת בנזיל הוא 91 גרם mol -1 . מאז יש טבעת בנזן, קבוצת בנזיל הוא ארומטי.במנגנונים של כימיה אורגנית, קבוצת בנזיל יכולה להיווצר או כקרבוקציה רדיקלית (C 6 H 5 CH 2 + ) או carboanion C 6 H 5 CH 2 - ). לדוגמה, בתגובות החלפה נוקלאופיליסטית, נוצרת רדיקלית benzylic או קטיון ביניים. יש התייצבות גבוהה יותר של אלה intermediates לעומת רדיקאל אלקיל או קטיון. התגובה של המיקום benzylic דומה לזה של עמדת allylic. קבוצות בנזיל משמשות לעתים קרובות בכימיה אורגנית כמו קבוצות מגן, במיוחד כדי להגן על חומצה carboxylic או אלכוהול קבוצות פונקציונליות. -> ->
מה ההבדל בין פניל בנזיל?• הנוסחה המולקולרית של פניל היא C
6 H 5 בעוד שבבנזל הוא C 6 H 5 CH < 2 . • בנזיל יש תוספת CH 2
קבוצה לעומת פניל. • בפניל, טבעת הבנזן מחוברת ישירות למולקולה תחליפית או לאטום, אך בבנזייל, קבוצת ה- CH 2
מקשרת את הקשר עם מולקולה אחרת או אטום.




