ההבדל בין S ו- P לחסום אלמנטים | S נגד אלמנטים בלוק
ההבדל מפתח - S לעומת אלמנטים של P P
ההבדל העיקרי בין רכיבי s ו- p יכול להיות מוסבר בצורה הטובה ביותר באמצעות התצורה האלקטרונית שלהם. באלמנטים של הבלוקים, האלקטרון האחרון מתמלא אל תת-המרכיבים של האלמנט ואלמנטים של בלוק p, האלקטרון האחרון ממלא את תת-הסוף. כאשר הם יוצרים יונים; s אלמנטים לחסום להסיר האלקטרונים שלהם מתוך subshell החיצוני בקלות ואילו אלמנטים לחסום p לקבל אלקטרונים p subshell p או להסיר אלקטרונים מ p-subshell. אלמנטים מסוימים של קבוצת p יוצרים יונים חיוביים המסלקים אלקטרונים מן החלק העליון p-subshell וכמה אלמנטים (האלמנטים electronegative ביותר) טופס יונים שליליים קבלת אלקטרונים מאחרים. כאשר אתה מחשיב את המאפיינים הכימיים, יש הבדל משמעותי בין s ו אלמנטים לחסום p; זה בעצם בגלל תצורת האלקטרון.
-> ->מה הם S- לחסום אלמנטים?
רכיבי S-block הם האלמנטים הכימיים בקבוצה I ובקבוצות II בטבלה המחזורית. מאז subhell זה יכול להכיל רק שני אלקטרונים, אלמנטים אלה בדרך כלל יש אחד (קבוצה I) או שניים (קבוצה II) אלקטרונים בקליפה החיצונית. המרכיבים בקבוצה I ו- II מוצגים למעלה בטבלה.
- diff מאמר בינוני לפני הטבלה ->| IA | II | |
| 2 | לי | |
| 3 | Na | Mg |
| 4 | K | C |
| 5 | Rb | Sr |
| 6 | Cs | Ba |
| 7 | מ | Ra |
| IA | מתכות אלקליות |
| II | מתכות אדמה אלקליין |
כל האלמנטים ב- S לחסום טופס יונים חיוביים והם מאוד תגובתי.
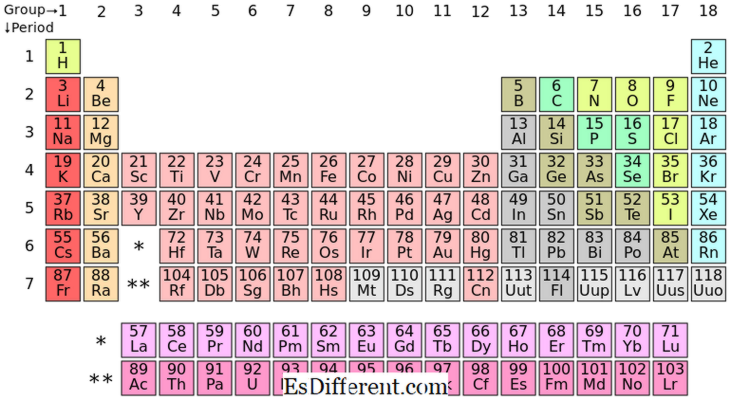
המיקום של רכיבי ה- S-Block בטבלה המחזורית
-> ->מה הם רכיבי P-Block?
אלמנטים P-block הם האלמנטים שהאלקטרון האחרון שלהם מתמלא לתוך תת-סף. ישנם שלושה p-orbitals; כל מסלול יכול להכיל שני אלקטרונים, מה שהופך את סך של שישה אלקטרונים p. לכן, אלמנטים p-block יש אחד עד שישה אלקטרונים p ב פגז החיצוני שלהם. P-Block מכיל גם מתכות וגם לא מתכות; בנוסף יש כמה metalloids מדי.
| 13 | 16 | 17 | 18 | 2 | B | |
| C | N | O | F Ne | 3 | אל | Si |
| P | S | Cl | Ar | 4 | Ga | Ge |
| Se | > | <<<<<<<<<<<<<<<<<<<<< > <<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<<< | תצורת Common Electron: | |||
| אלמנטים S-Block: | אלמנטים S- בלוק יש תצורה אלקטרונים נפוצים של ns גז | 1 | (עבור קבוצה אני אלמנטים) ו [גז אצילי] ns | 2 | (עבור אלמנטים קבוצה II). | אלמנטים P-Block: |
| אלמנטים P-block יש תצורה אלקטרונית נפוצה של n [גז אצילי] | 2 | np | 1-6 | . אבל, הליום יש 1s | 2 | תצורה; זה מצב מיוחד. |
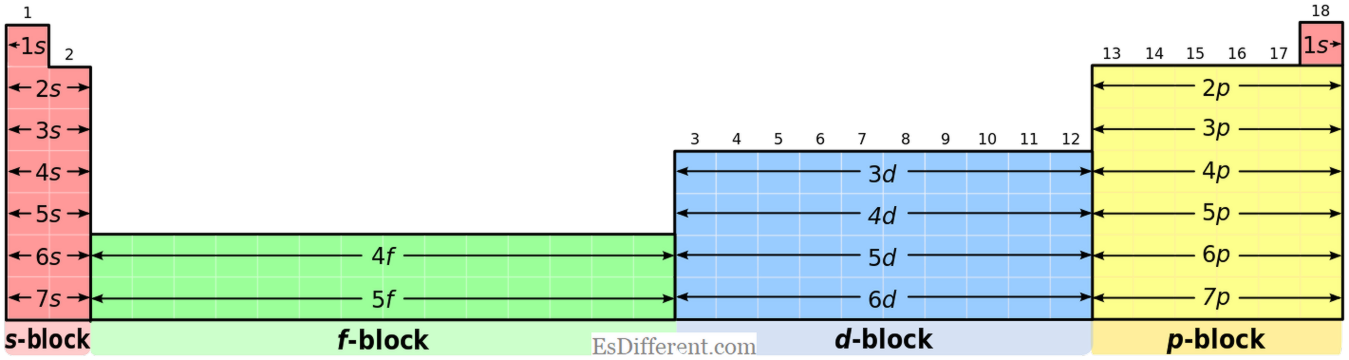
חמצון מדינות:
S- לחסום אלמנטים:
אלמנטים לחסום S לא מראים מצבי חמצון מרובים כמו אלמנטים לחסום p. לדוגמה, הקבוצה אני אלמנטים מראים 1 + מצב חמצון אלמנטים קבוצה II מראים מצב חמצון +2. בניגוד אלמנטים של בלוק s, אלמנטים לחסום p יש מצב חמצון משותף עבור הקבוצה המתאימה שלהם בטבלה המחזורית וכמה מדינות חימצון נוספות, בהתאם ליציבות של היון. 13 14 15 16 17
18 כללי תצורת אלקטרונים ns 2 np 1 np np
2
ns 2
np 3



