ההבדל בין ואלנסי ואלנס אלקטרונים | ואלנסי לעומת ואלנס אלקטרונים
הבדלים מרכזיים - Valency לעומת ואלנס אלקטרונים
ואלנטי אלקטרונים ואלקטרונים ערכיות הם מונחים הקשורים זה לזה, ואת
ההבדל העיקרי בין valency ואלקטרונים electron הוא הסביר ביותר בהגדרות שלהם; valence electrons הם האלקטרונים שבקליפה החיצונית ביותר של אלמנט בעוד אלקטרונים הם מספר האלקטרונים שיש לקבל או להסיר כדי להגיע לתצורת הגז האצילית הקרובה ביותר זהו האלקטרונים שבקליפה החיצונית שבדרך כלל תורמים ליצירת קשרים כימיים. באטומים מסוימים, מספר האלקטרונים הערכיות שווה למספר האלקטרונים הערכיים. -> -> מה הם אלנס אלקטרונים?
מספר האלקטרונים בקליפה החיצונית של האטום נקרא "אלקטרונים ערכיות". מסיבה זו, את הקליפה החיצונית של אטום נקרא "פגז valence". רוב הזמן, אלה הם האלקטרונים, אשר לוקחים חלק מליטה כימית. כאשר אלמנטים יוצרים קטיונים, הם מסירים אלקטרונים מקליפת הערכיות. מספר האלקטרונים הערכיות באלמנט קובע את הקבוצה בטבלה המחזורית.-> -> מה הם ואלנסי אלקטרונים?
מספר האלקטרונים הנדרש כדי להרוויח או להפסיד כדי למלא את הקליפה החיצונית של אטום נקרא "אלקטרונים valency". עבור אטום מסוים, מספר האלקטרונים valency תלוי במספר אלקטרון האלקטרון באטום. עבור נתרן, valency שווה 1, כי זה מסיר את האלקטרון האחרון בקליפה החיצונית כדי להשיג מבנה אוקטט של גז אצילי הקרוב.

- diff מאמר לפני הטבלה ->
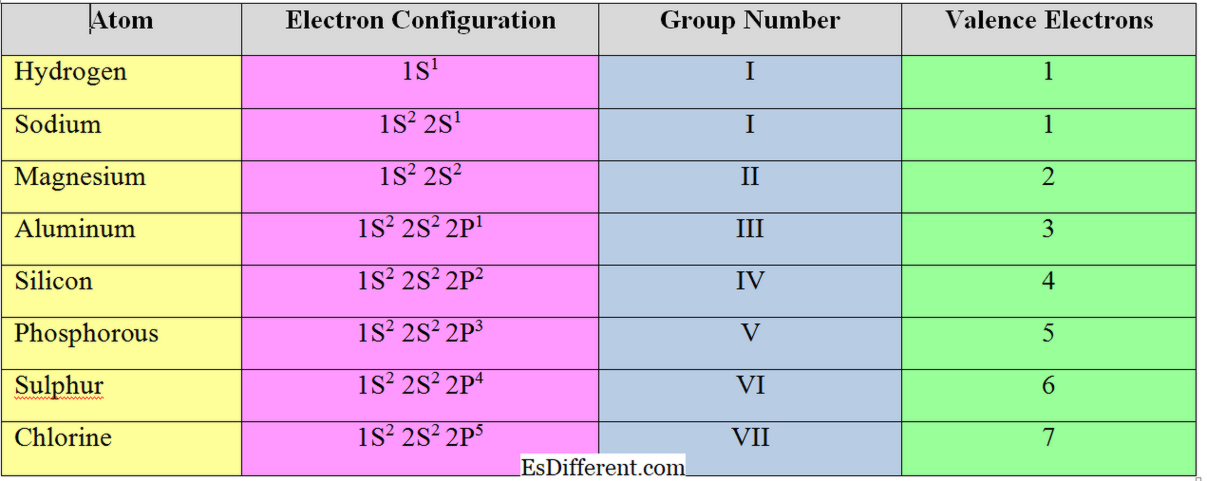
Valency של אלמנטים קבוצתיים עיקריים
עבור אלמנטים ממתכת, מספר ואלנטי אלקטרונים = מספר ואלנס אלקטרונים
|
האלקטרונים בקליפה החיצונית של האטום נקראים "אלקטרונים ערכיות". עבור "s" ו "p" אלמנטים הקבוצה, מספר אלקטרונים valence שווה למספר הקבוצה שלהם.
דוגמה
ואלנטי אלקטרונים: מספר האלקטרונים שיש לקבל או להסיר כדי להשיג את תצורת האלקטרון של גז אצילי הקרוב נקרא "אלקטרונים valency" או "valence" של אטום.
באופן כללי, עבור אלמנטים מתכתיים (אלמנטים בקבוצה I, II ו- III), מספר אלקטרונים הערכיות שווה למספר אלקטרונים valency; הם מסירים את האלקטרונים בקליפת הערכיות כדי להשיג את מבנה האוקט.
אבל, אלמנטים שאינם מתכת מקבלים אלקטרונים כדי להשיג את תצורת האלקטרון של הגז האצילי הקרוב ביותר. לכן, הערכים של אלמנטים מתכתיים מחושבים על ידי הפחתת סך אלקטרונים הערכיות מ 8. עבור כלור, מספר אלקטרונים valency = 8-7 = 1
מאפייני Valency ואלנס אלקטרונים
Valency ו ואלנס אלקטרונים של אלמנטים השמיני של הקבוצה
ואלנס אלקטרונים:

אלמנטים קבוצה VIII הם גזים אצילי, והם יציבים מבחינה כימית. הקונכייה החיצונית שלהם שלמה, והיא מכילה שמונה אלקטרונים בקונכייה החיצונית ביותר (למעט הליום-הי); כך קבוצה VIII electrons יש שמונה אלקטרונים valence.
Valency אלקטרונים:
Valency הוא מדד ליכולת ליצור קשרים עם אלמנטים או מולקולות אחרות. גזים אצילים אינם מקבלים או מסלקים אלקטרונים כדי להשיג את חוק האוקטטים, שכן הם כבר השלימו את הקונכייה האחרונה. לכן, את הערכים של אלמנטים השביעי הקבוצה שווה לאפס. Image באדיבות:
"פגז אלקטרונים 010 ניאון - ללא תווית" על ידי קומון: משתמש: פומבה (עבודה מקורית על ידי commons: משתמש: גרג רובסון) - // commons. wikimedia. org / wiki / קטגוריה: Electronic_shell_diagrams (גרסה שכותרתה המקביל). (CC BY-SA 2. 0 בבריטניה) באמצעות




