ההבדל בין EDTA ו- EGTA
EDTA לעומת EGTA
EDTA ו- EGTA הן סוכני chelating. שניהם חומצות carboxylic polyamino ויש להם פחות או יותר את אותם מאפיינים.
EDTA
EDTA הוא השם המקוצר של חומצה tethraacetic ethylene דיאמין. זה ידוע גם בשם (ethylene dinitrilo) חומצה tetraacetic. להלן המבנה של EDTA.
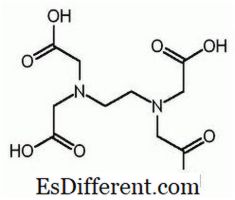
מולקולת EDTA יש שישה אתרים שבהם יון מתכת יכול להיות מחויב. ישנן שתי קבוצות אמינו וארבע קבוצות carboxyl. שני אטומי חנקן של קבוצות אמינו יש זוג אלקטרונים unshared בכל. EDTA הוא ליגנד hexadentate. כמו כן, הוא סוכן chelating בשל היכולת להטות מתכות יונים. EDTA צורות chelates עם כל קטיונים למעט מתכות אלקליות אלה chelates יציבים מספיק. היציבות נובעת מהאתרים המורכבים שבמולקולה, המוליכים לכלוב כמו סביב יון המתכת. זה מבודד את יון המתכת ממולקולות ממס, ובכך למנוע את הפיתרון. קבוצת carboxyl של EDTA יכול לנתק פרוטונים לתרום; לכן, EDTA יש תכונות חומצי. מינים שונים של EDTA מקוצרים כמו H 4 Y, H 3 > - , 2 Y 2, HY3 - ו- Y 4- . ב pH נמוך מאוד (בינוני חומצי), את הטופס פרוטוני של EDTA (H 4 Y) הוא השולט. לעומת זאת, ב pH גבוה (בינוני בסיסי), דפרוטייטד טופס מלא (Y 4 ) שולט. וכמו השינויים pH מ pH נמוך ל pH גבוה, צורות אחרות של EDTA לשלוט בערכי pH מסוימים. EDTA זמין בצורת protonated מלא או בצורת מלח. דיסודיום EDTA וסידן סידן EDTA הם צורות המלח הנפוצות ביותר הזמינים. חומצה חופשית H 4 Y ואת התייבשות של מלח נתרן Na 2 H 2 Y. 2H 2 O זמינים מסחרית באיכות מגיב.
EGTA EGTA הוא מונח מקוצר עבור אתילן גליקול tetraacetic חומצה. זהו סוכן chelating, ו דומה מאוד EDTA.EGTA יש זיקה גבוהה יותר עבור יוני סידן מאשר יונים מגנזיום. EGTA יש את המבנה הבא.
בדומה EDTA, EGTA יש גם ארבע קבוצות carboxyl, אשר יכול לייצר ארבעה פרוטונים על ניתוק. ישנן שתי קבוצות amine ואת שני אטומי חנקן של קבוצות אמינו יש unshared זוג אלקטרונים בכל אחד. EGTA יכול לשמש חיץ כדי להידמות ה- pH של תא חי. תכונה זו של EGTA היתרי השימוש שלה טיהור זיקה טיהור, המהווה טכניקה טיהור חלבון.

מה ההבדל בין